Moleküle auf Sendung
Die Natur nutzt Botenstoffe, um Informationen zu übermitteln. Wie sich das für medizinische Therapien und in der Technik nutzen lässt, untersuchen der Ingenieur Robert Schober und etliche Forschungsgruppen aus sehr unterschiedlichen Wissenschaftsdisziplinen.
In der modernen Nachrichtentechnik oder zum Beispiel auch in der medizinischen Diagnose mit Computer- und Magnetresonanz-Tomografie werden Informationen normalerweise mit elektromagnetischen Wellen übertragen. „Im Gewebe von Menschen und Tieren stoßen elektromagnetische Wellen jedoch rasch an Grenzen“, sagt Robert Schober. „Diese Hürden möchten wir mithilfe biologischer Signalwege überwinden.“
Der Ingenieur ist Inhaber des Lehrstuhls für Digitale Übertragung an der FAU und Sprecher des Graduierten-Kollegs „Synthetische molekulare Kommunikation über unterschiedliche Größenordnungen“ (SyMoCADS). Dieses von der Deutschen Forschungsgemeinschaft (DFG) geförderte Vorhaben will die technische Informationsübertragung in lebende Organismen hinein erweitern und dabei auf die deutlich smarteren Methoden setzen, die die Evolution in vielen Jahrmillionen hervorgebracht hat: „In der Biologie werden Informationen häufig über Moleküle weitergegeben“, erklärt Schober. „Nach diesem Vorbild wollen wir biologische Mechanismen, Hormone und Pheromone, Signalmoleküle und Geruchsstoffe nutzen, um beispielsweise Krebs besser bekämpfen zu können.“
Hühnereier für die Tumorforschung

Gerade die Krebsforschung und vor allem die äußerst schwierige Behandlung dieser heimtückischen Krankheiten zeigt sehr deutlich, wie wichtig und oft genug lebensrettend die biologische Kommunikation ist. Ursache und Grundlage von bösartigen Tumoren sind Zellen aus dem eigenen Organismus der betroffenen Menschen. Häufig wird der Krebs nicht rechtzeitig entdeckt. Eine Operation entfernt dann zwar einen sehr großen Teil, aber oft genug leider nicht alle der gefährlichen Tumorzellen. Diese gezielt zu eliminieren, ist immer eine Gratwanderung: In sehr vielen Bereichen funktionieren sie genauso wie normale Körperzellen – Maßnahmen gegen Tumorzellen können daher leicht auch gesundes Gewebe treffen.
Ein Ausweg aus dem Dilemma zwischen einer erfolgversprechenden Krebsbehandlung und gefährlichen Nebenwirkungen sind Maßnahmen, die genau auf die verbliebenen Tumorzellen zielen. „Das gelingt zum Beispiel dann besonders gut, wenn man versteht, wie die Krebszellen mit dem Rest des Organismus kommunizieren“, sagt Robert Schober. „Bislang lässt sich das oft nur mithilfe von Tierversuchen erforschen.“ Um das zu ändern, fördert ein bis 2026 laufendes Projekt des Bundesministeriums für Bildung und Forschung (BMBF) eine Alternative: Gemeinsam mit Silke Härteis und ihrer Gruppe von der Universität Regensburg sowie einem Team der Technischen Hochschule Deggendorf nutzt eine Gruppe vom FAU-Lehrstuhl für Digitale Übertragung Hühnereier, um Krebsgewebe am Leben zu erhalten und es so genauer zu untersuchen.
„In diesem System kann man beobachten, wie und auf welchen Wegen Wirkstoffe das Tumorgewebe erreichen“, erklärt Robert Schober. Dazu sollen zunächst Farbstoffe in das Blutgefäßsystem der Hühnereier eingebracht und deren Ausbreitung untersucht werden. Kennt man diese Zusammenhänge, lassen sich leichter Wirkstoffe designen, die später in einem Krebspatienten selbstständig zu einem Tumor finden und dabei möglichst geringe Nebenwirkungen zeigen.
Von Magneten ins Ziel gelenkt
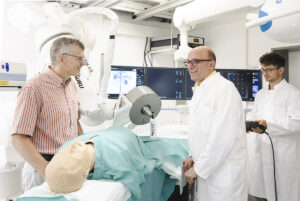
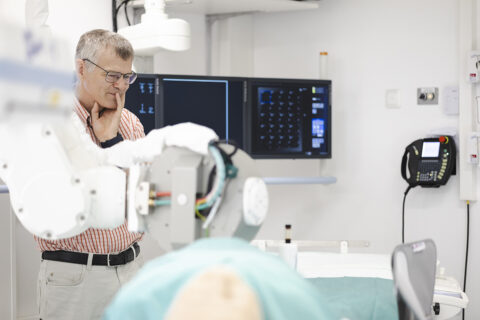
Das DFG-Graduierten-Kolleg SyMoCADS setzt in seinen Projekten allerdings nicht nur auf die biologische Kommunikation. Auch Magnetfelder sollen dabei helfen, Krebsmedikamente zum Zielort zu bringen. Dazu wird der Wirkstoff an Nanopartikel geheftet, die aus superparamagnetischem Eisenoxid bestehen. Wird diese Kombination in Blutgefäße gespritzt, kann in der Sektion für Experimentelle Onkologie und Nanomedizin (SEON) am Uniklinikum Erlangen ein starker Magnet auf einem mechanischen Arm die Substanz zu den Krebszellen steuern. Liegt ein Tumor nahe an der Körperoberfläche, funktioniert diese Methode in Tierversuchen bereits gut.
Bei der Verbesserung dieses Therapieansatzes könnten die Maschinenbau-Labors der FAU eine wichtige Rolle spielen. Das klingt zunächst recht verblüffend, ist aber durchaus konsequent: Um einen Tumor möglichst effizient zu bekämpfen, müssen die magnetischen Nanopartikel mit dem Wirkstoff durch die Blutgefäße zu ihrem Ziel gelangen. Das wiederum ist in einem sehr komplexen System mit zum Teil winzigen Kapillargefäßen eine echte Herausforderung. Also schaut sich das SyMoCADS-Teilprojekt solche Tumoren genau an und baut sie dann mit 3D-Druckern aus durchsichtigem Kunststoff nach. In diesen Modellen können sich auch die Steuer-Algorithmen in der Praxis bewähren, die von der FAU-Elektrotechnik in einem weiteren Projekt ausgetüftelt wurden.
Befindet sich ein Tumor tiefer im Inneren des Organismus, sollte man zunächst einmal seine genaue Position bestimmen, um danach eine Behandlung zu ermöglichen. Eine SyMoCADS Projektgruppe aus dem Bereich der Bioverfahrenstechnik nutzt für diese Suche „Vesikel“ genannte, winzig kleine Biogefäße, die bereits in anderen Bereichen als Mini-Bioreaktoren eingesetzt werden. Dank eines geschickten Design und mit geeigneten Wirkstoffen in ihrem Inneren sollen diese Biogefäße nicht nur einen Tumor finden, sondern auch seine Lage verraten. Mit solchen Vesikeln sollen dann auch Substanzen für eine Krebstherapie treffsicher an ihr Ziel transportiert werden, um genau dort freigesetzt zu werden.
Außerdem rechnet ein weiteres Projekt am FAU-Lehrstuhl für Digitale Übertragung aus, wie diese Mikro-Biogefäße gestaltet werden können, um möglichst gut zu arbeiten. „Eine solche Bündelung sehr unterschiedlicher Disziplinen ist nicht nur in der Krebsforschung, sondern auch in vielen anderen Wissenschaftsbereichen sehr erfolgversprechend“, erklärt Robert Schober.
Einige Köpfe hinter der Forschung
Autor: Roland Knauer
Dieser Artikel ist Teil des FAU Magazins
 Innovation, Vielfalt und Leidenschaft – so lauten die drei Grundwerte unserer FAU, so sind sie in unserem Leitbild festgehalten. An der FAU leben wir diese Grundwerte jeden Tag
Innovation, Vielfalt und Leidenschaft – so lauten die drei Grundwerte unserer FAU, so sind sie in unserem Leitbild festgehalten. An der FAU leben wir diese Grundwerte jeden Tag
und in allem, was wir tun – in der Forschung, in der Lehre und wenn es darum geht, Wissen, das an der Universität entsteht, in die Gesellschaft hineinzutragen.
Die zweite Ausgabe unseres FAU Magazins macht dies einmal mehr sichtbar: Es zeigt Forschende, die immer wieder die Grenzen des bislang Machbaren überschreiten. Es stellt Studierende vor, die gemeinsam Höchstleistung für ihre FAU erbringen, erzählt von Lehrenden, die mit Freude und Kreativität ihr Wissen weitergeben. Und es berichtet von Mitarbeiterinnen und Mitarbeitern, die sich mit Weitblick und einem Gespür fürs Wesentliche der (Forschungs-)Infrastruktur an der FAU widmen sowie von Menschen in Schlüsselpositionen, die für ihre Universität da sind und sich für den Forschungsstandort stark machen.
Download: FAU Magazin (PDF) Weitere Artikel online lesen